Saggio alla fiamma di cloruri, il modello atomico di Bohr
In questa lezione di laboratorio viene trattato il saggio alla fiamma. Si tratta di un metodo di riconoscimento dei sali che per i cloruri funziona particolarmente bene.
Cloruro di Sodio (Na), Bario (Ba), Calcio (Ca), Potassio (K), Litio (Li) ed infine Stronzio (Sr) sono stati utilizzati in questo esperimento.
All’apparenza tali cloruri si presentano come delle comuni polveri bianche.

Materiali Utilizzati
• Bacchetta di vetro con filo in metallo• Becco Bunsen
• Sali (Cloruri di Na, Ba, Ca, K, Li, Sr)
• Acido cloridrico
• Acqua distillata
• Beuta
• Vetrini da orologio (uno per cloruro)
• Accendino/strumento per accendere il becco Bunsen
Procedimento
- Collegare il becco Bunsen ad un tubo del gas metano
- (Se presente) Girare la valvola per permettere il flusso del gas
- Accendere il becco Bunsen con l’accendino
- Diluire l’acido cloridrico con l’acqua distillata già immessa nella beuta almeno al 90%
- Ripulire la bacchetta di vetro con il filo metallico da eventuali residui
Per ogni cloruro analizzato
- Aggiungere pochi grammi del cloruro nel rispettivo vetrino da orologio
- Intingere la punta del filo metallico nel vetrino da orologio
- Avvicinare la bacchetta alla fiamma blu del Becco Bunsen
- Ripulire la bacchetta dai residui del cloruro
Attenzione: Non permettere alla fiamma di toccare il vetro della bacchetta, potrebbe fondere!
Ripulire la bacchetta
- Intingere il filo metallico nella beuta contenente acido cloridrico
- Inserire il filo metallico nella fiamma del becco Bunsen
- Ripetere il procedimento finché le fiamme non si colorano più di verde primaverile
Osservazioni
La fiamma del becco Bunsen, alimentato, nel nostro caso, da una bombola di metano, ha un interno di colore blu scuro, avvolto in piccole fiammelle giallo-rosse.
Il colore della fiamma varia appena viene messa a contatto con il metallo impolverito di cloruri, diventando rosso, verde, giallo e perfino violetto!
Inoltre, abbiamo notato che questi colori ricordano quelli dei fuochi d’artificio, che sono, appunto, composti anche di cloruri.
Per ogni cloruro abbiamo eseguito la procedura di analisi, ed annotato eventuali osservazioni, riportate in questa tabella.
| Cloruro | Colore Osservato | Eventuali osservazioni |
|---|---|---|
| Sodio | Arancione | — |
| Bario | Arancione | Secondo gli altri del gruppo, fiamma di colore giallo-verde |
| Calcio | Rosso intenso | Secondo la prof ci sono anche piccole fiamme gialle. |
| Potassio | Un tocco di viola | — |
| Litio | Rosso carminio | Ricorda un colore magenta |
| Stronzio | Rosso intenso. | — |
Infine, la professoressa ci ha comunicato i colori “corretti” da essere osservati, riferendosi ad un libro.
Ne abbiamo sbagliati circa due, probabilmente perché il processo di pulizia del filo metallico fu eseguito solo parzialmente: il filo metallico deve essere immerso più volte nell’acido cloridrico e nella fiamma per ottenere migliori risultati, evitando l’accumulo di residui.
| Cloruro | Colore fiamma | Eventuali annotazioni |
|---|---|---|
| Sodio | Giallo | Le mani acquistano tinta cadaverica, quando esposte verso luce al sodio, come quella dei lampioni vecchi. Tinta cadaverica significa che non si riescono a distinguere i colori, il giallo sovrasta tutto. |
| Bario | Verde pisello | . |
| Calcio | Rosso mattone | Sprazi rossi in una fiamma giallastra |
| Potassio | Violetto | — |
| Litio | Rosso carminio | . |
| Stronzio | Rosso scarlatto | Non persistente, ossia la fiamma colorata non dura a lungo. |
Chi effettuò il saggio alla fiamma con considerevoli risultati?
Quello che abbiamo fatto oggi lo ha fatto Niels Bohr all’inizio del XX secolo, esaminando lo spettro di emissione a righe (ossia la luce prodotta in stato incandescente) dell’idrogeno. Infatti Bohr concepì il suo modello di atomo basandosi sul saggio alla fiamma dell’idrogeno ed utilizzando calcoli quantistici.
Dunque quando si parla di spettro a righe si intende la gamma dei colori, ossia le varie onde emesse da un corpo se portato all’incandescenza.
Bohr calcola con un’ equazione le distanze delle orbite, e la conseguente generazione di colori, spiegata sotto. Tali distanze, dunque i colori prodotti,combaciano perfettamente solo con I’idrogeno, con nessun altro atomo.
Tale modello, sebbene contenga più di un errore concettuale, essendo una sorta di ibrido tra la fisica tradizionale e quella quantistica, viene ancora utilizzato per la chimica semplice, infatti funziona perfettamente per gli argomenti spiegati sul libro di biologia, ma noi, per passione della scienza, compiremo un excursus storico su tutti i modelli atomici.
Proviamo ad effettuare una spiegazione
Avviso: in questa spiegazione viene usata la fisica quantistica. È un argomento introdotto da poco, ho cercato di riportare il contenuto del libro ed applicarlo a questo esperimento in un modo semplice da comprendere, nonostante ciò la difficolta di comprensione del testo da qui in poi aumenterà notevolmente.
Possiamo provare a spiegare la colorazione della fiamma attraverso il modello atomico di Bohr, successore del modello di Rutherford. Come esso ha
- Un nucleo composto da neutroni e protoni
- Orbite di elettroni attorno al nucleo
Innanzitutto, Bohr, per questo modello utilizza i fondamenti della fisica quantistica, considerando anche le due nature della luce: ondulatoria e corpuscolare.
Considerandone la natura ondulatoria, le onde di energia (luce) hanno frequenza e lunghezza d’onda inversamente proporzionali: $ c = \lambda * \ni$. Considerandone la natura corpuscolare, una volta che la luce interagisce con la materia, arrivano tanti pacchetti di fotoni, che eccitano la materia fornendo quantità $x*n$ di energia, con $n$ che rappresenta numero di pacchetti di energia ricevuti. Quando questi pacchetti sono hanno una frequenza maggiore alla frequenza di limite, vengono liberati elettroni, che si tramutano in luce
Ogni elemento gassoso oppure reso gassoso ha uno spettro di emissione a righe, che fornisce dati su quali onde emette se, ad esempio, viene portato ad incandenscenza attraverso la fiamma del becco Bunsen.
Attraverso calcoli quantistici, Rutherford deduce che l’elettrone normalmente viaggia su un’orbita, attorno al nucleo.
Questa orbita viene detta stazionaria. Se l’elettrone ottiene energia - ad esempio sottoforma di calore - per dissiparla, esso cambia orbita, ed inizia ad orbitare in un’orbita più lontana ed ampia della precedente.
Le orbite sono quantizzate, ossia l’elettrone riesce solo una volta accumulata almeno una quantità d’energia $x$ a cambiare orbita, un po’come l’altezza necessaria con cui alzare la gamba al fine salire un gradino delle scale; se è minore, non è possibile oltrepassare il gradino.
Se alzo più il piede, riesco a salire più gradini alla volta, così come un elettrone riesce a scalare più di un’orbita data una maggiore quantità di energia.
Per continuare su un’orbita più ampia di quella stazionaria, però, è necessario un dispendio costante d’energia: quando l’elettrone esaurisce l’energia ricavata sottoforma di calore, torna nell’orbita stazionaria, rilasciando, per ogni orbita scalata l’energia come fotone, ossia sottoforma di luce.
Conosciamo l’equazione dell’effetto fotoelettrico scoperto da Einstein, in particolare la natura ondulatoria della luce, quando eccita delle particelle di metallo e ne provoca la ionizzazione.
Infatti l’equazione $E=h*\ni$, in cui l’energia è pari alla costante di Planck per la frequenza, ossia il numero di oscillazioni dell’onda al secondo dimostra una relazione di diretta proporzionalità tra frequenza ed energia.
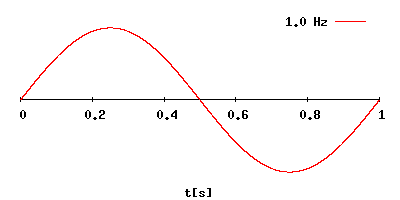
La frequenza viene misurata in Hertz (Hz), ossia numero di oscillazioni dell’onda al secondo.
Nello spettro del visibile, visibile appunto all’occhio umano, le lunghezze d’onda maggiori (~700nm) - dunque onde di frequenza ed energia minori - formano il rosso, mentre le minori (~400nm) - onde di frequenza ed energia maggiori - il blu.
Ne consegue che se gli elettroni ricevono più energia, allora emetteranno una luce blu, mentre se ne ricevono meno, emetteranno una luce rossa.
In ogni caso dopo questa discussione non sappiamo ancora perché la quantità di energia ricevuta dagli elettroni appartenenti ad atomi di differenti solfati varia, ma solo la correlazione tra energia, colore ed orbite saltate dall’elettrone, per spiegare il tutto ipotizzo che avremo bisogno di un diverso modello atomico.
Il modello di Bohr è in grado di spiegare le radiazioni emesse dall’atomo di Idrogeno, un atomo molto semplice, con un solo elettrone, ma non riesce a giustificare lo spettro a righe degli altri elementi.
- Citazione da Dalla struttura atomica all’elettrochimica, II edizione
Altri post correlati di Scienze naturali:
Le leggi dei gas ideali: Gay-Lussac, Boyle e la legge generale dei...
Vita di Lavoisier
Calcinazioni con metalli, LSS Nascita della Chimica Moderna
Le reazioni chimiche che abbiamo scoperto in questo percorso LSS fino ad...
Altre calcinazioni
Questo è il mio sito web personale contenente i Compiti Scolastici e gli appunti presi da me, Andrea Bortolotti, durante il liceo. Ci sono numerose materie, tra cui Fisica, Chimica, Latino, Inglese, Geometria, Storia dell' Arte e tante altre ancora! L' ho creato per essere più ordinato e per non perdere nulla.
CC BY-NC-ND 4.0





